Дисулфит

| |

| |
| Систематско име | пентаксиди-1κ3O,2κ2O-дисулфат(S—S)(2−)[1] |
Други називи метабисулфитен јон | |
| Назнаки | |
|---|---|
| 23134-05-6 | |
| ChemSpider | 140610 |
| |
| 3Д-модел (Jmol) | Слика |
| PubChem | 159940 |
| |
| UNII | 7992SO049K |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Конјуг. киселина | Дисулфурна киселина |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Дисулфит, попознат како метабисулфит или пиросулфит, ― хемиско соединение кое го содржи јонот S2O2−
5. Тоа е безбоен дијанион кој првенствено се продава во облик на натриум метабисулфит или калиум метабисулфит. Кога се раствораат во вода, овие соли го ослободуваат водородсулфитот HSO−
3 анјон. Овие соли делуваат еднакво на натриум хидрогенсулфит или калиум хидрогенсулфит.[2]
Структура
[уреди | уреди извор]За разлика од дисулфатот (S2O2−
7), дисулфитен јон (S2O2−
5) има несиметрична структура со S-S врска. Состојбата на оксидација на атомот на сулфур поврзан со 3 атоми на кислород е +5 додека оксидациониот број на другиот атом на сулфур е +3.[3]
Анјонот се состои од SO2 група поврзана со SO3 група, со негативниот полнеж повеќе месен на SO3 крајот. Должината на врската S-S е 2,22 Å, а „тионатските“ и „тионитските“ S–O растојанија се 1,46 и 1,50 Å редоследно.[4]
Производство
[уреди | уреди извор]Солите на дисулфитниот јон се произведуваат со дехидрација на соли на водородсулфитен јон (HSO−
3). Кога растворите на натриум хидрогенсулфит или калиум хидрогенсулфит се испаруваат, се добива натриум метабисулфит и калиум метабисулфит.[5]
Иако рамнотежата лежи далеку лево, испарувањето на бисулфитната сол ќе произведе значителна количина дисулфит.[6]
Дисулфитот е конјугирана база на дисулфурна киселина (пиросулфурна киселина), која потекнува од сулфурна киселина во согласност со реакцијата на дехидрација погоре:
- 2 H2SO3 → 2 HSO−
3 + 2 H+ → H2S2O5 + H2O
Дисулфитниот јон, исто така, произлегува од додавањето на сулфур диоксид во сулфитниот јон:
| HSO− 3 3 + H+ SO32− + SO2 5 |
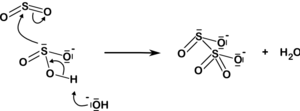 |
Употреба
[уреди | уреди извор]Дисулфитните соли се користени за зачувување на храна и пијалоци.
Примери на дисулфити
[уреди | уреди извор]- Натриум метабисулфит (Е223) и калиум метабисулфит (Е224) користени како конзерванс и антиоксиданс во храната. Сулфитите се вмешани во астматските реакции и исто така може да предизвикаат симптоми кај неастматските лица, имено дерматит, сугреб, црвенило, хипотензија, стомачна болка и пролив, па дури и анафилакса опасна по живот.[7]
Наводи
[уреди | уреди извор]- ↑ 1,0 1,1 Меѓународен сојуз за чиста и применета хемија (2005). Номенклатура на неорганска хемија (Препораки на МСЧПХ од 2005 година). Cambridge (UK): КХД–МСЧПХ. ISBN 0-85404-438-8. стр. 130. Електронска верзија.
- ↑ Johnstone, H. F. (1946). „Sulfites and Pyrosulfites of the Alkali Metals“. Inorganic Syntheses. Inorganic Syntheses. 2. стр. 162–167. doi:10.1002/9780470132333.ch49. ISBN 9780470132333.
- ↑ Lindqvist, I.; Mörtsell, M. „The Structure of Potassium Pyrosulfite and the Nature of the Pyrosulfite Ion". Acta Crystallogr. (1957“. 10: 406–409. doi:10.1107/S0365110X57001322. Наводот journal бара
|journal=(help) - ↑ K. L. Carter, T. A. Siddiquee, K. L. Murphy, D. W. Bennett "The surprisingly elusive crystal structure of sodium metabisulfite" Acta Crystallogr. (2004).
- ↑ „Sulfites, Thiosulfates, and Dithionitesl Chemistry“, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH
- ↑ Bassam Z. Shakhashiri: Chemical demonstrations: a handbook for teachers of chemistry The University of Wisconsin Press, 1992, стр.9
- ↑ „Adverse reactions to the sulphite additives“. Gastroenterol Hepatol Bed Bench. 5 (1): 16–23. 2012. PMC 4017440. PMID 24834193.
